高脂血症容易得糖尿病吗
1人回复
问题描述:
高脂血症容易得糖尿病吗
医生回答专区 因不能面诊,医生的建议仅供参考
高脂血症患者确实更容易患糖尿病,两者存在密切的代谢关联。高脂血症可能通过胰岛素抵抗、脂肪组织炎症、游离脂肪酸毒性、β细胞功能损伤、遗传因素等机制增加糖尿病风险。
1、胰岛素抵抗血液中过高的甘油三酯和低密度脂蛋白胆固醇会干扰胰岛素信号传导,导致肌肉、肝脏等组织对胰岛素的敏感性下降。这种情况下胰腺需要分泌更多胰岛素来维持血糖稳定,长期超负荷工作可能引发β细胞功能衰竭。
2、脂肪组织炎症内脏脂肪过度堆积时会分泌肿瘤坏死因子α等炎症因子,这些物质可阻断胰岛素受体活性。同时巨噬细胞浸润脂肪组织形成的慢性低度炎症状态,会进一步加剧全身胰岛素抵抗现象。
3、游离脂肪酸毒性高脂血症患者血液中游离脂肪酸浓度持续升高,这些脂质分子可在非脂肪组织如肝脏、胰腺中异常沉积。在胰腺内,脂毒性会直接损伤β细胞的胰岛素分泌功能,导致血糖调节能力下降。
4、β细胞功能损伤长期暴露于高脂环境会使胰腺β细胞中线粒体功能紊乱,内质网应激反应激活,最终引发细胞凋亡。尸检研究显示糖尿病患者的β细胞数量可比健康人减少过半,这与脂代谢异常密切相关。
5、遗传因素某些基因变异如PPARγ、FTO等可能同时影响脂代谢和糖代谢通路。具有这些遗传背景的个体,在高脂饮食等环境因素作用下,更易出现高脂血症与糖尿病共病的情况。
对于高脂血症患者,建议定期监测空腹血糖和糖化血红蛋白水平,控制每日脂肪摄入量在总热量的30%以内,优先选择深海鱼、坚果等富含不饱和脂肪酸的食物。每周保持150分钟以上中等强度有氧运动,如快走、游泳等有助于改善胰岛素敏感性。已出现糖耐量异常者可在医生指导下使用二甲双胍等药物进行早期干预。同时需要避免吸烟、过量饮酒等加重代谢紊乱的不良生活习惯。
相似问题
推荐 用糖皮质激素会引起高脂血症吗
长期或大剂量使用糖皮质激素可能引起高脂血症。糖皮质激素通过影响脂肪代谢、促进肝脏合成甘油三酯等机制导致血脂异常,但短期规范用药通常不会显著升高血脂。 糖皮质激素可能通过多种途径导致血脂水...
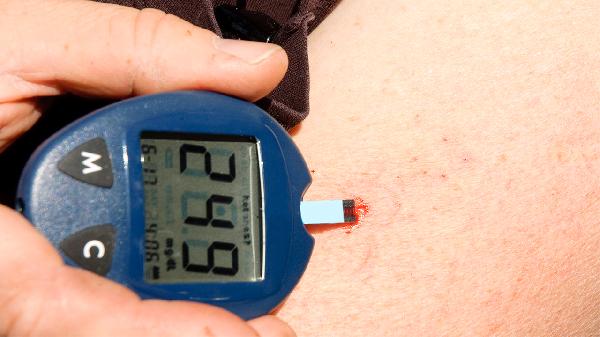
为什么肥胖的人容易得糖尿病
肥胖与糖尿病之间的关系紧密,肥胖者更容易患上糖尿病,主要原因包括身体脂肪过多和胰岛素抵抗等。过多的脂肪会导致身体代谢功能异常,进而引发血糖升高,同时,脂肪堆积还会导致胰岛素抵抗,使得血糖难以被有效利用。为了降低患病风险,肥胖者应在医生指导下积极管理体重。1、身体脂肪过多:肥胖者体内脂肪含量较高,容易导致代谢紊乱,进而引起血糖水平升高。体重指数(BMI)超过3...
科普推荐 为你持续推送健康知识
药物性心肌病的治疗方法有哪些
药物性心肌病可通过调整用药、营养支持、药物治疗、心脏康复训练、手术治疗等方式干预。药物性心肌病通常由长期使用蒽环类化疗药、抗精神病药、免疫抑制剂、违禁药物或过量摄入兴奋剂等因素引起,可能表现为心律失常、心力衰竭、心肌纤维化等症状。1、调整用药立即停用或替换致病药物是首要措施,例如蒽环类化疗药多柔比星需根据心功能监测结果调整剂量。临床常用右雷佐生等心脏保护剂减...
修复胃黏膜口服液
修复胃黏膜口服液通常包括康复新液、铝碳酸镁混悬液、胶体果胶铋干混悬剂、硫糖铝口服混悬液、枸橼酸铋钾颗粒等药物,需在医生指导下根据具体病因选择使用。胃黏膜损伤可能与饮食刺激、药物因素、幽门螺杆菌感染、慢性胃炎、胃溃疡等因素有关。一、康复新液康复新液含美洲大蠊提取物,能促进胃黏膜组织修复,适用于胃溃疡及慢性胃炎引起的黏膜损伤。该药物可改善局部微循环,加速创面愈合...
腰椎颈椎病外敷药有哪些
腰椎颈椎病外敷药主要有氟比洛芬凝胶贴膏、双氯芬酸二乙胺乳胶剂、消痛贴膏、活血止痛膏、洛索洛芬钠贴剂等。腰椎颈椎病多与慢性劳损、退行性变、受寒等因素有关,表现为局部疼痛、活动受限等症状,外敷药物可缓解炎症和疼痛,但需在医生指导下使用。一、氟比洛芬凝胶贴膏氟比洛芬凝胶贴膏属于非甾体抗炎药,适用于腰椎颈椎病引起的轻至中度疼痛。该药物通过皮肤吸收直接作用于疼痛部位,...
戴美瞳会长寄生虫吗
戴美瞳一般不会长寄生虫,但若清洁不当或使用劣质产品可能增加眼部感染风险。美瞳属于角膜接触镜,其安全隐患主要与微生物感染有关,寄生虫感染概率极低。规范使用合格的美瞳产品并做好日常护理时,寄生虫感染风险可忽略不计。角膜接触镜相关感染通常由细菌或真菌引起,常见于镜片清洁不彻底、超时佩戴、储存盒污染等情况。选择具有医疗器械注册证的正规产品,每日佩戴不超过8小时,使用...
血糖多高眼睛才会模糊需要做手术
血糖超过11.1毫摩尔每升可能出现眼睛模糊,但多数情况无须手术,仅严重糖尿病视网膜病变需激光或玻璃体切割术治疗。血糖升高导致眼睛模糊的机制主要与高血糖损伤视网膜微血管有关。短期血糖波动超过11.1毫摩尔每升时,晶状体渗透压改变可引起暂时性视力模糊,此时通过控制血糖多可恢复。长期未控制的高血糖会引发糖尿病视网膜病变,早期表现为微血管瘤和点状渗出,此时仍以药物治...
小儿生长发育最快的时期是哪个阶段?
小儿生长发育最快的时期是婴儿期,尤其是出生后的第一年。婴儿期生长发育速度较快,通常表现为体重、身高、头围等指标迅速增长。婴儿期是小儿生长发育的关键阶段,出生后的前12个月是体重增长最快的时期。新生儿出生时平均体重为3千克左右,到1岁时体重可达到出生时的3倍。身高增长同样显著,出生时平均身长为50厘米,1岁时可增长25厘米左右。头围在出生后的前6个月增长较快,...
1个月婴儿胎毒怎么去除
1个月婴儿出现胎毒症状时,一般无须特殊治疗,可通过日常护理逐渐缓解。胎毒通常指新生儿脂溢性皮炎或湿疹等皮肤问题,可能与母体湿热体质、遗传因素或环境刺激有关。1、温水清洁每日用37-40℃温水轻柔清洗婴儿皮肤褶皱处,避免使用碱性肥皂。清洗后及时擦干水分,可配合无香料婴儿润肤乳保持皮肤湿润。家长需注意动作轻柔,防止摩擦加重皮肤损伤。2、衣物选择选择纯棉透气的衣物...
心脏回血不足会出现什么情况
心脏回血不足通常是指心脏舒张功能减退或静脉回流受阻导致的心输出量减少,可能引发胸闷、乏力、呼吸困难等症状。心脏回血不足可能与心肌缺血、心力衰竭、心脏瓣膜病等因素有关,需结合具体病因进行干预。1、胸闷气短心脏回血不足时,肺部血液循环受阻可能导致氧气交换效率下降,表现为活动后胸闷或静息时气短。部分患者伴随胸部压迫感,尤其在爬楼梯或情绪激动时加重。此类症状需与呼吸...
静息心率49正常吗
静息心率49次/分是否正常需结合个体情况判断,健康成年人静息心率通常为60-100次/分,但长期运动人群或特定生理状态下可能出现低于60次/分的窦性心动过缓。运动员或长期进行高强度有氧训练的人群,静息心率可低至40-50次/分,这是心脏功能增强的表现。这类人群通常伴随窦性心律齐、无头晕乏力等症状,心电图检查显示无传导阻滞或其他异常。睡眠期间心率自然下降,部分...
骨转移不能吃的食物有哪些
骨转移患者应避免高盐、高脂、高糖及刺激性食物,主要包括腌制食品、油炸食品、碳酸饮料、酒精饮品等。骨转移多由恶性肿瘤扩散引起,可能伴随骨质破坏、疼痛等症状,饮食需兼顾营养支持与疾病控制。一、高盐食物腌制食品如咸菜、腊肉含大量钠盐,过量摄入可能加重钙质流失,不利于骨骼修复。骨转移患者常合并高钙血症,需限制每日盐分摄入,建议选择新鲜蔬菜替代。二、高脂食物油炸食品、...
男人爱到什么程度会吃醋
男人吃醋的程度通常与情感投入深度和安全感缺失有关,当感受到关系中的潜在威胁时,可能表现出从轻微不安到强烈占有欲的醋意反应。吃醋行为主要受性格差异、关系阶段、信任基础、过往经历、沟通模式等因素影响。1、性格差异内向敏感型男性更容易因伴侣的社交行为产生醋意,可能将中性互动误解为暧昧信号;外向自信者通常醋意阈值较高,但过度自负也可能因面子问题突然爆发激烈反应。九型...

扁平疣中医能治好吗
扁平疣通过中医治疗通常能取得较好效果,中医治疗方式主要有中药外敷、火针疗法、艾灸、内服汤药、穴位贴敷等。扁平疣多由湿热毒蕴、气血失和或外感邪毒所致,表现为皮肤表面扁平丘疹,表面光滑或粗糙。1、中药外敷马齿苋、板蓝根、大青叶等清热解毒中药煎汁湿敷患处,可抑制病毒复制。将药材煮沸后取滤液冷却,用纱布浸透药液敷于疣体,每日重复进行。外敷药物可直接作用于病灶,对局部...

女孩子怎样保护自己的身体
女孩子保护身体清洁、心理健康和生理健康是维护整体健康的关键,主要涉及个人卫生习惯、安全意识培养、营养均衡、适度运动和定期体检等方面。一、个人卫生保持会阴清洁是预防感染的基础,每日用温水清洗外阴,避免使用刺激性洗液。经期及时更换卫生巾,选择透气棉质内裤。洗澡后擦干皮肤褶皱处,防止真菌滋生。口腔卫生需刷牙两次并使用牙线,定期检查牙齿。二、安全防护外出避免独行夜路...
扇形草莓是什么原因
扇形草莓通常由授粉不均、温度异常、水分失调、营养失衡或病虫害等因素引起。草莓在生长过程中若出现形态异常,多与栽培管理或环境因素有关,需针对性调整种植条件。1、授粉不均草莓花朵若未能充分授粉,会导致果实发育不均衡。蜜蜂等传粉昆虫不足、花期遭遇连续阴雨天气均可能影响授粉效果。人工辅助授粉或增加蜂箱可改善此类问题,确保果实均匀膨大。2、温度异常花期或幼果期遭遇低温...

鼻子周围毛孔变大原因
鼻子周围毛孔变大可能由油脂分泌旺盛、皮肤老化、角质堆积、紫外线损伤、不当护肤等原因引起。毛孔粗大通常表现为皮肤表面可见的圆形或椭圆形凹陷,可能伴随黑头或粉刺。1、油脂分泌旺盛皮脂腺活跃会导致毛孔被动扩张以排出多余皮脂。青春期、高温环境或高糖高脂饮食可能加剧这一现象。建议使用温和洁面产品清洁,避免过度去油刺激皮脂腺反弹分泌。含有水杨酸或烟酰胺的护肤品有助于调节...

谈什么样的恋爱性价比最高 恋爱有什么好谈的
恋爱性价比最高的关系通常是双方在情感支持、共同成长和生活目标上高度契合的伴侣关系。健康的恋爱能带来情绪价值提升、社会支持强化、自我认知完善等积极影响,主要有平等沟通、三观匹配、需求互补、成长同步、边界清晰五个特征。一、平等沟通关系中的对话模式直接影响情感消耗程度。高频有效的沟通能减少误解成本,避免因猜忌产生的情绪内耗。双方采用非暴力沟通方式表达需求时,恋爱中...

2月草莓为何要尽量少吃
2月草莓建议尽量少吃,主要与反季节种植的农药残留风险、营养含量下降、口感偏酸等因素有关。反季节草莓可能因催熟技术影响品质,且冬季病虫害防治用药量增加,需谨慎选择正规渠道产品。2月上市的草莓多为温室大棚反季节栽培,自然光照和积温不足可能导致糖分积累较少,果实酸度较高。部分农户为加速成熟会使用植物生长调节剂,虽符合国家标准但过量摄入可能对敏感人群产生刺激。冬季低...

女孩子如何保护自己的身体
女孩子保护身体需要从生理卫生、心理健康、疾病预防等多方面综合管理,主要包括保持清洁习惯、均衡饮食、规律运动、定期体检、建立安全意识等措施。1、生理卫生每日用温水清洗会阴部,避免使用刺激性洗液。经期及时更换卫生巾,选择透气棉质内裤。发育期开始后需进行乳房自检,观察是否有异常肿块或分泌物。注意口腔卫生,早晚刷牙并使用牙线清洁牙缝。2、营养管理保证优质蛋白摄入,如...
引体向上可以锻炼肱二头肌吗
引体向上可以锻炼肱二头肌,但主要发力肌群为背阔肌和上肢屈肌群。肱二头肌在动作过程中作为协同肌参与发力,其刺激程度取决于握距、动作速度和身体倾斜角度等因素。采用反握窄距引体向上时,肱二头肌的激活程度会显著提升。这种变式要求手掌朝向面部,双手间距小于肩宽,肘关节屈曲幅度增大,迫使肱二头肌承担更多负荷。动作过程中保持躯干垂直地面,避免借助惯性摆动,能更精准地刺激目...
科室问题
一级
二级
二级
二级
二级
二级
二级
二级
医生推荐
医院推荐
最新问答 更多
-
全身红是怎么回事
#全科#
-
孩子上周四确诊疱疹性咽峡炎还有轻微咳嗽咋办
#小儿外科#
-
阿司匹林维生素C咀嚼片与哪些药不宜同时服用
#保健科#
-
纵膈肿瘤如何解决严重吗
#肿瘤内科#
-
被跳蚤咬了用什么药膏
#药剂科#
-
左耳轻微耳鸣怎么回事
#耳鼻喉科#
-
脱肛还能缩回去吗
#肛肠科#
-
新生儿黄疸值18正常吗
#新生儿黄疸#
-
o型血输血输什么型
#血液科#
-
肾积水会头晕头痛吗
#肾内科#
-
血小板350严重吗
#全科#
-
治疗抑郁的方法有哪些
#心理咨询科#
-
毒虫咬了肿了怎么办
#全科#
-
有糖尿病可以吃一点红吗
#糖尿病#
-
心肌梗死病人会抽筋吗
#心血管内科#
行业资讯 2025年08月21日 星期四

- 4种被误认为升压,实则适合高血压患者的肉类,错过可惜!
- 从134斤减到104斤,掉秤30斤后总结:减肥就是不断重复这6件事
- 久坐危害大!50岁后每天这样动一动,远离腰酸背痛和慢性病
- 为何白头发越长越多?自以为是老了,医生:或是缺乏3种营养素
- 冬季吃什么食物补肾 教你如何补肾壮阳?


